“神農嘗百草,一日而遇七十毒”,形象記錄了中藥起源于人類對各種新鮮藥材(鮮藥)的認識。晉代葛洪《肘後備急方》中“青蒿一握,水二升漬,搗絞汁,盡服之”,對于鮮藥利用的記載,成為諾貝爾生理學或醫學獎獲得者屠呦呦發現青蒿素的思想理論源泉。鮮藥未經加工,保持了天然狀态,但對于鮮藥的科學認識還極其有限。
人參(Panax ginseng C. A. Mey)為“百草之王”。味甘微寒,具大補元氣,複脈固脫,補脾益肺,生津安神之功效,東西方都應用廣泛。2019年11月27日,南京中醫藥大學曹鵬研究員團隊在腫瘤免疫治療協會(SITC)官方雜志Journal for ImmunoTherapy of Cancer(免疫學1區, IF: 8.676)在線發表論文“Ginseng-derived nanoparticles alter macrophage polarization to inhibit melanoma growth”, 該文首次報道了從新鮮人參中提取的囊泡通過極化巨噬細胞,抑制黑色素腫瘤的生長。本文的通訊作者為曹鵬研究員,第一作者為曹萌副研究員,助理研究員顔懷江和博士研究生韓暄等人參與了研究工作。

細胞外囊泡(extracellular vesicles,EVs)是由細胞分泌的納米尺寸的脂質膜封閉結構。EVs作為細胞間通訊的重要介質,影響生理和病理狀況。鑒于其轉移生物活性成分和克服生物屏障的能力,EVs越來越多地被探索為潛在的治療劑。目前對于細胞外囊泡的研究,主要集中在哺乳動物細胞上清液和體液,而植物,特别是藥用植物囊泡領域的研究十分有限。
曹鵬研究團隊從2016年開始開展了中藥鮮藥的研究,發現從新鮮人參的汁液中可以提取到類似于動物細胞分泌的胞外囊泡,并将這種囊泡命名為Ginseng-derived nanoparticles(GDNPs)。研究人員發現這種人參來源的植物囊泡的直徑為300 nm左右。多組學分析顯示,GDNPs富含多種人參來源的蛋白、脂類、核酸和小分子。

![]()
研究發現GDNPs對單核-巨噬細胞有着很強的親嗜性,能夠被巨噬細胞有效地吞噬,同時促進巨噬細胞向具有抗腫瘤作用的M1型巨噬細胞極化,并且極化的巨噬細胞分泌大量ROS殺傷腫瘤。經過進一步的分析,證實GDNPs極化巨噬細胞的主要機制是通過其含有的神經酰胺(Ceramide)活化巨噬細胞表面的Toll樣受體4(TLR4)。荷瘤小鼠實驗結果表明GDNPs的治療有效促進腫瘤微環境中的腫瘤相關巨噬細胞(tumor associated macrophage,TAM)向抗腫瘤的M1型巨噬細胞極化,解除腫瘤微環境免疫抑制狀态,活化CD8+T淋巴細胞和NK細胞,抑制黑色素瘤的生長。
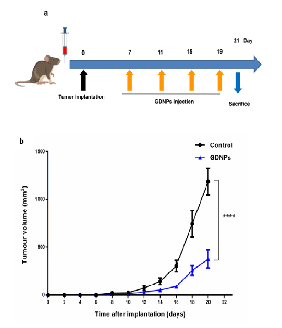

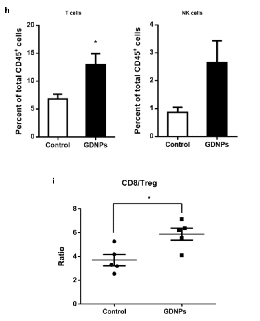
該研究首次發現囊泡是鮮藥人參發揮藥效的重要物質基礎,加深了對中藥的科學認識,為拓展鮮藥利用途徑帶來新的啟示; 同時也是首次發現藥用植物來源的囊泡具有重編程腫瘤相關巨噬細胞的功能,GDNPs對于腫瘤的免疫治療可能帶來新的希望。



